कैंसर के खिलाफ नई उम्मीद: भारतीय वैज्ञानिकों ने खोजा “स्लीपिंग” एंजाइम का रहस्य!
Cell surface receptors like Receptor Tyrosine Kinases (RTK) are crucial for converting extracellular signals (from chemical cues like growth factors, generally referred to as ligands) to tightly regulated cellular response. Ligand binding to extracellular receptors activates intracellular coupled enzymes (tyrosine kinases). The activated enzyme, in turn, adds phosphate group to several tyrosine molecules that function as an adaptor for assembling a signalling complex. The formation of the signalling complex regulates diverse cellular functions like cell growth, development, and host immune response. Spontaneous activation of RTKs, in the absence of ligands, is often linked to multiple human pathologies like cancers, diabetes, and autoimmune disorders. Researchers are exploring how a cell maintains an autoinhibited state of the enzyme and why such autoinhibition is breached during the progression of human pathology.
-Edited by Jyoti Rawat-
कल्पना कीजिए, आपकी कोशिकाओं की सतह पर कुछ “दरवाजे” (रिसेप्टर) होते हैं, जो बाहर से आने वाले विकास के संकेतों को पकड़ते हैं और कोशिका को बताते हैं – “बढ़ो, विभाजित हो जाओ!” लेकिन जब ये दरवाजे बिना किसी संकेत के भी खुद-ब-खुद खुल जाते हैं, तो कोशिकाएं बेकाबू होकर बढ़ने लगती हैं – यही तो कैंसर है!
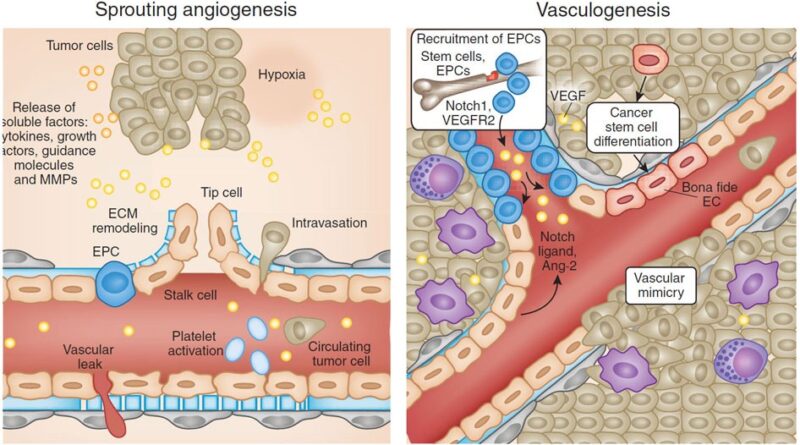
अब सबसे रोमांचक हिस्सा: VEGFR परिवार के रिसेप्टर नई रक्त वाहिकाओं (एंजियोजेनेसिस) बनाने के मास्टरमाइंड होते हैं। ट्यूमर को बढ़ने के लिए ऑक्सीजन और पोषण चाहिए, तो ये रिसेप्टर ट्यूमर के आसपास नई खून की नलियां बनवा देते हैं।
लेकिन इस परिवार में दो सदस्य बहुत अलग हैं:
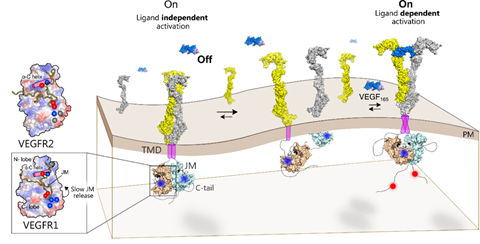
- VEGFR2 – बिना संकेत के भी “ऑन” हो जाता है और तेजी से काम करता है।
- VEGFR1 – ये “चालाक जासूस” की तरह है! खुद को “मृत एंजाइम” बनाकर छिपा लेता है। भले कोशिका में कितनी भी उथल-पुथल हो, ये खुद सक्रिय नहीं होता। बल्कि VEGF-A से 10 गुना ज्यादा मजबूती से बंधता है, लेकिन सिर्फ हल्की-सी झलक दिखाता है।
कोलकाता के IISER (Indian Institute of Science Education and Research) के डॉ. राहुल दास और उनकी टीम ने इस रहस्य को सुलझाया। उन्होंने पाया कि VEGFR1 में एक अनोखा “आयनिक लैच” (इलेक्ट्रोस्टैटिक लैच) होता है, जो सिर्फ इसी में मौजूद है। ये लैच जक्स्टामेम्ब्रेन सेगमेंट को काइनेज डोमेन से “हुक” की तरह जोड़ देता है और VEGFR1 को ऑटोइनहिबिटेड (खुद को रोकने वाली) स्थिति में स्थिर रखता है।
यानी, VEGFR1 एक तरह से “स्लीपिंग मॉड” में रहता है – निष्क्रिय, लेकिन तैयार! ये खोज बताती है कि कोशिका कैसे सामान्य हालत में कैंसर को रोकती है।
और सबसे रोमांचक बात – इस खोज से नया इलाज का रास्ता खुल सकता है! अगर हम छोटे-छोटे अणुओं से VEGFR1 की इस निष्क्रिय अवस्था को और मजबूत करें, तो कोलन कैंसर (कोलोरेक्टल कार्सिनोमा) और गुर्दे के कैंसर जैसी बीमारियों में ट्यूमर की रक्त वाहिकाओं का निर्माण रोका जा सकता है। VEGFR1 की अनियंत्रित सक्रियता से कैंसर में दर्द, ट्यूमर कोशिकाओं का जीवित रहना और फैलना होता है – इसे कंट्रोल करने से नई थेरेपी आ सकती है।
ट्यूमर कैसे नई रक्त वाहिकाएं बनवाता है ट्यूमर ऑक्सीजन की कमी (हाइपोक्सिया) महसूस करता है → एंजियोजेनिक फैक्टर्स छोड़ता है → नई रक्त वाहिकाएं बनती हैं → ट्यूमर बढ़ता और फैलता है।
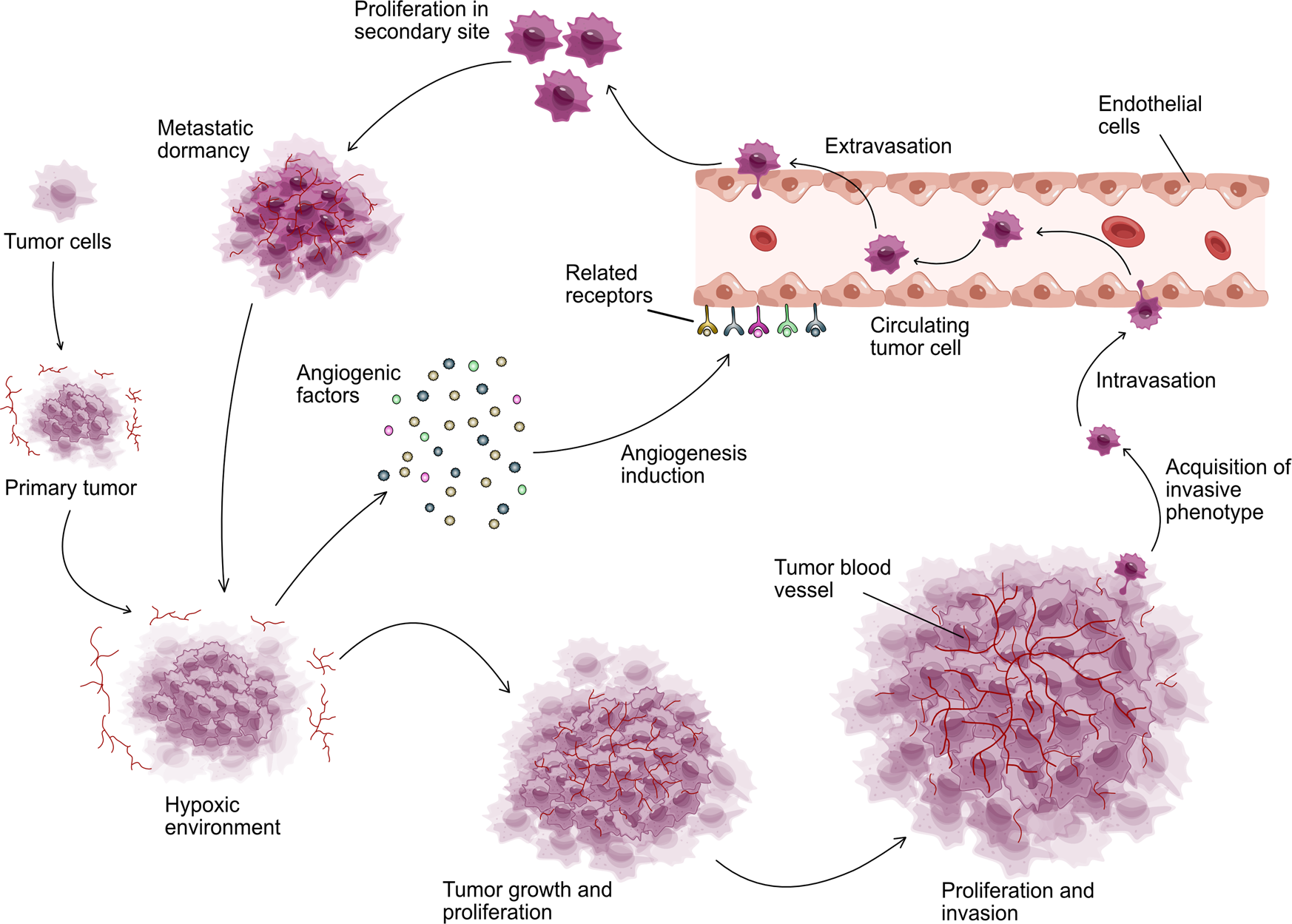
कैंसर के इलाज में नया रास्ता अगर हम छोटे अणुओं से VEGFR1 की इस “स्लीपिंग” या निष्क्रिय अवस्था को और मजबूत कर दें, तो ट्यूमर की रक्त आपूर्ति रुक सकती है। इससे कोलन कैंसर (कोलोरेक्टल) और गुर्दे के कैंसर में ट्यूमर का विकास, दर्द, कोशिकाओं का जीवित रहना और फैलना रोका जा सकता है।
ये शोध Nature Communications जर्नल में फरवरी 2024 में प्रकाशित हुआ है। टीम ने ITC और स्टॉप्ड-फ्लो फ्लोरीमीटर जैसी एडवांस तकनीकों से साबित किया कि टायरोसिन फॉस्फेट भी इस प्रक्रिया में महत्वपूर्ण भूमिका निभाता है।
संक्षेप में, एक “मृत” दिखने वाला एंजाइम असल में कैंसर का दुश्मन बन सकता है! भारतीय वैज्ञानिकों की ये खोज कैंसर के इलाज में नया अध्याय लिख सकती है। क्या पता, आने वाले सालों में इसी आधार पर नई दवाएं बाजार में आएं और लाखों जिंदगियां बचें।
====================================================
(स्रोत: IISER Kolkata की रिसर्च, Nature Communications में प्रकाशित अध्ययन)