कोशिका के भीतर कैंसर रोधी तंत्र की एक सूक्ष्म खोज
by-jyoti rawat
आधुनिक जीव विज्ञान में शोधकर्ताओं ने कोशिका की सतह पर मौजूद एक अत्यंत महत्वपूर्ण आणविक प्रक्रिया का अनावरण किया है। यह खोज मुख्य रूप से ‘सेल सरफेस रिसेप्टर्स’ पर केंद्रित है, जो कोशिका के भीतर वृद्धि कारकों (Growth Factors) को व्यवस्थित करने, कोशिकाओं के विभाजन, उनके अस्तित्व, चयापचय और एक स्थान से दूसरे स्थान तक जाने की प्रक्रिया को नियंत्रित करते हैं। इस जटिल तंत्र का सबसे महत्वपूर्ण हिस्सा एक एंजाइम संरचना है जो कैंसर जैसी घातक बीमारियों को रोकने में सक्षम है। आईआईएसईआर (IISER) कोलकाता के वैज्ञानिकों ने विशेष रूप से ‘रिसेप्टर टायरोसिन किनेसेस’ (RTK) नामक रिसेप्टर्स की भूमिका को स्पष्ट किया है, जो बाहरी रासायनिक संकेतों को कोशिका के भीतर एक सुव्यवस्थित प्रतिक्रिया में बदलने का कार्य करते हैं।
रिसेप्टर टायरोसिन किनेसेस और सिग्नलिंग की प्रक्रिया
सेल सरफेस रिसेप्टर्स कोशिका के द्वारपाल की तरह कार्य करते हैं। जब बाहर से कोई रासायनिक संकेत, जिसे ‘लिगैंड’ कहा जाता है, इन रिसेप्टर्स से जुड़ता है, तो कोशिका के अंदर मौजूद एंजाइम (टायरोसिन किनेसेस) सक्रिय हो जाते हैं। यह सक्रिय एंजाइम कोशिका के भीतर फॉस्फेट समूहों को जोड़कर एक ‘सिग्नलिंग कॉम्प्लेक्स’ तैयार करते हैं। यही कॉम्प्लेक्स तय करता है कि कोशिका का विकास कैसे होगा और हमारी प्रतिरक्षा प्रणाली किस प्रकार प्रतिक्रिया देगी। सामान्य परिस्थितियों में यह प्रक्रिया पूरी तरह नियंत्रित होती है, लेकिन यदि लिगैंड की अनुपस्थिति में भी ये रिसेप्टर्स खुद-ब-खुद सक्रिय हो जाएं, तो यह शरीर में कैंसर, मधुमेह और स्व-प्रतिरक्षित विकारों जैसी गंभीर समस्याओं को जन्म देता है।
वीईजीएफआर परिवार का रहस्यमय व्यवहार
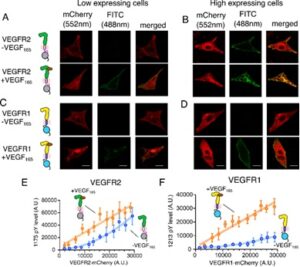
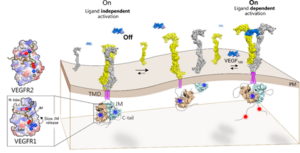
शोध के दौरान वैज्ञानिकों का ध्यान वैस्कुलर एंडोथेलियल ग्रोथ फैक्टर रिसेप्टर (VEGFR) परिवार पर केंद्रित हुआ, जो नई रक्त वाहिकाओं के निर्माण (एंजियोजेनेसिस) के लिए जिम्मेदार है। यह प्रक्रिया घाव भरने और भ्रूण के विकास के लिए जितनी आवश्यक है, ट्यूमर के विकास के लिए उतनी ही खतरनाक भी हो सकती है। शोधकर्ता इस बात को लेकर चकित थे कि इस परिवार के दो प्रमुख सदस्य, VEGFR1 और VEGFR2, एक जैसे होने के बावजूद बिल्कुल अलग व्यवहार करते हैं। जहाँ एक ओर VEGFR2 बिना किसी बाहरी संकेत के भी स्वतः सक्रिय होकर रक्त वाहिकाओं का निर्माण शुरू कर सकता है, वहीं VEGFR1 अधिक सांद्रता होने पर भी तब तक सक्रिय नहीं होता जब तक उसे लिगैंड का आदेश न मिले। यह रिसेप्टर एक ‘शांत एंजाइम’ के रूप में व्यवहार करता है और अपने साथी की तुलना में कहीं अधिक मजबूती से संकेतों को पकड़ता है।
आयनिक लैच: शरीर का प्राकृतिक सुरक्षा लॉक
डॉ. राहुल दास और उनकी टीम ने इस पहेली को सुलझाते हुए पाया कि VEGFR1 की इस निष्क्रिय और नियंत्रित अवस्था के पीछे एक विशेष ‘आयनिक लैच’ (Ionic Latch) का हाथ है। यह लैच केवल VEGFR1 में ही पाया जाता है और एक आणविक हुक की तरह कार्य करता है जो एंजाइम को उसकी ‘ऑटोइनहिबिटेड’ यानी स्वयं-अवरुद्ध अवस्था में स्थिर रखता है। यह सुरक्षा तंत्र ही वह कारण है जिससे कोशिका अनियंत्रित रूप से विभाजित होने से बची रहती है। जब यह तंत्र ठीक से काम करता है, तो कैंसर कोशिकाओं को बढ़ने के लिए आवश्यक संकेत नहीं मिल पाते। शोधकर्ताओं ने यह भी प्रस्तावित किया कि कोशिका के भीतर मौजूद ‘टायरोसिन फॉस्फेट’ इस गतिविधि को नियंत्रित करने में महत्वपूर्ण भूमिका निभाते हैं, जो कैंसर के उपचार के लिए एक नया चिकित्सीय मार्ग खोल सकते हैं।
भविष्य की चिकित्सा और कैंसर का समाधान
नेचर कम्युनिकेशन जर्नल में प्रकाशित यह अध्ययन कोलोरेक्टल (आंत) और गुर्दे के कैंसर के इलाज की दिशा में एक बड़ी उम्मीद जगाता है। यदि वैज्ञानिक ऐसे छोटे अणु (Small Molecules) विकसित करने में सफल होते हैं जो VEGFR1 की इस ‘ऑटोइनहिबिटेड’ या निष्क्रिय अवस्था को और अधिक स्थिर कर सकें, तो कैंसर की कोशिकाओं को बढ़ने से रोकना संभव हो जाएगा। यह तकनीक विशेष रूप से उन रोगात्मक स्थितियों में प्रभावी होगी जहाँ रक्त वाहिकाओं का अनियंत्रित निर्माण ट्यूमर को पोषण प्रदान करता है। इस प्रकार, शरीर के अपने ही ‘सुरक्षा लॉक’ को मजबूत करके हम बिना किसी भारी दुष्प्रभाव के कैंसर जैसी बीमारियों का मुकाबला करने की दिशा में आगे बढ़ सकते हैं।
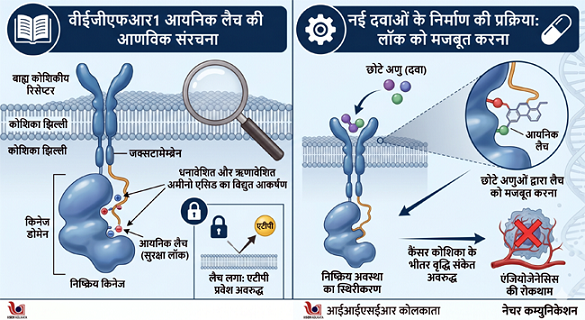
‘आयनिक लैच’ की सूक्ष्म आणविक संरचना
कोशिका के भीतर मौजूद रिसेप्टर्स को एक मशीन की तरह माना जा सकता है। VEGFR1 नामक इस रिसेप्टर में एक ‘किनेज डोमेन’ होता है, जो ऊर्जा के स्रोत (ATP) का उपयोग करके संकेतों को आगे भेजता है। ‘आयनिक लैच’ इसी मशीन का एक सुरक्षा पिन है।
आणविक स्तर पर, यह लैच धनावेशित (Positive) और ऋणावेशित (Negative) अमीनो एसिड के बीच एक मजबूत विद्युत आकर्षण (Electrostatic Attraction) से बनता है। शोधकर्ताओं ने पाया कि VEGFR1 के ‘जक्सटामेम्ब्रेन’ (Juxtamembrane) हिस्से में कुछ विशेष अमीनो एसिड होते हैं जो किनेज डोमेन के ऊपर एक भौतिक अवरोध की तरह चिपक जाते हैं।
जब तक यह लैच लगा रहता है, एंजाइम की सक्रिय साइट ‘बंद’ रहती है, जिससे ATP वहां प्रवेश नहीं कर पाता और सिग्नलिंग रुकी रहती है। यह संरचना इतनी विशिष्ट है कि यह VEGFR1 को उसके सहोदर VEGFR2 से अलग करती है, जिसमें इस प्रकार का सुरक्षा तंत्र नहीं पाया जाता।
नई दवाओं के निर्माण की प्रक्रिया: ‘लॉक’ को मजबूत करना
इस खोज ने दवा कंपनियों और वैज्ञानिकों के लिए एक नया ‘टारगेट’ (Drug Target) प्रदान किया है। पारंपरिक कैंसर दवाएं अक्सर सक्रिय एंजाइम को रोकने की कोशिश करती हैं, लेकिन यह शोध “प्रिवेंटिव ब्लॉकिंग” पर जोर देता है। इसकी प्रक्रिया कुछ इस प्रकार होगी:
-
छोटे अणुओं (Small Molecules) की पहचान: वैज्ञानिक कंप्यूटर सिमुलेशन के माध्यम से ऐसे रसायनों की खोज कर रहे हैं जो ‘आयनिक लैच’ के पास जाकर फिट हो सकें। इन अणुओं का काम लैच के बंधन को और अधिक मजबूत बनाना होगा ताकि वह आसानी से न खुले।
-
निष्क्रिय अवस्था का स्थिरीकरण (Stabilization): दवा का उद्देश्य रिसेप्टर को उसकी ‘ऑटोइनहिबिटेड’ (Inhibited) स्थिति में ही जमा देना है। यदि रिसेप्टर निष्क्रिय अवस्था में स्थिर हो जाता है, तो कैंसर कोशिका के भीतर वृद्धि के संकेत पहुंचना बंद हो जाएंगे।
-
विशिष्टता (Specificity): चूँकि यह आयनिक लैच केवल VEGFR1 में मौजूद है, इसलिए इस पर आधारित दवाएं केवल इसी रिसेप्टर को प्रभावित करेंगी। इससे शरीर की अन्य स्वस्थ कोशिकाओं पर होने वाले दुष्प्रभाव (Side Effects) काफी कम हो जाएंगे।
चिकित्सा में इसका संभावित प्रभाव
नई दवाओं के निर्माण की यह प्रक्रिया विशेष रूप से ‘एंजियोजेनेसिस’ (Angiogenesis) को रोकने में क्रांतिकारी साबित हो सकती है। कैंसर ट्यूमर अपनी वृद्धि के लिए नई रक्त वाहिकाएं बनाने का प्रयास करते हैं। यदि हम दवाओं के जरिए VEGFR1 के आयनिक लैच को लॉक कर दें, तो ट्यूमर को रक्त की आपूर्ति करने वाली वाहिकाओं का निर्माण रुक जाएगा, जिससे ट्यूमर ‘भूखा’ रहकर सिकुड़ने लगेगा।
यह शोध न केवल कैंसर, बल्कि अन्य बीमारियों जैसे कि ‘मैकुलर डिजनरेशन’ (आंखों की बीमारी जहाँ अनियंत्रित रक्त वाहिकाएं दृष्टि बाधित करती हैं) के इलाज में भी एक नई उम्मीद लेकर आया है।
==============================================
लेख का लिंक: https://doi.org/10.1038/s41467-024-45499-2