कैंसर के इलाज में बड़ी कामयाबी: वैज्ञानिकों ने ढूँढा ‘सोते हुए’ एंजाइम का रहस्य
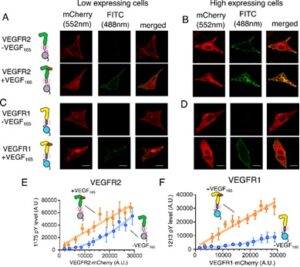
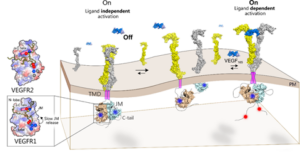
Cell surface receptors like Receptor Tyrosine Kinases (RTK) are crucial for converting extracellular signals (from chemical cues like growth factors, generally referred to as ligands) to tightly regulated cellular response. Ligand binding to extracellular receptors activates intracellular coupled enzymes (tyrosine kinases). The activated enzyme, in turn, adds phosphate group to several tyrosine molecules that function as an adaptor for assembling a signalling complex. The formation of the signalling complex regulates diverse cellular functions like cell growth, development, and host immune response. Spontaneous activation of RTKs, in the absence of ligands, is often linked to multiple human pathologies like cancers, diabetes, and autoimmune disorders. Researchers are exploring how a cell maintains an autoinhibited state of the enzyme and why such autoinhibition is breached during the progression of human pathology.

–ज्योति रावत –
चिकित्सा विज्ञान के क्षेत्र में कोलकाता स्थित भारतीय विज्ञान शिक्षा और अनुसंधान संस्थान (IISER) के शोधकर्ताओं ने एक ऐसी अभूतपूर्व खोज की है जो भविष्य में कैंसर के उपचार की दिशा बदल सकती है। यह शोध विशेष रूप से कोलन (मलाशय) और गुर्दे के कैंसर से जूझ रहे रोगियों के लिए एक नई उम्मीद लेकर आया है। इस शोध का केंद्र बिंदु ‘वीईजीएफआर1’ (VEGFR1) नामक एक एंजाइम है, जिसे वैज्ञानिक जगत में लंबे समय से एक रहस्यमयी पहेली माना जाता रहा है। आम भाषा में समझें तो हमारे शरीर की कोशिकाओं की सतह पर कुछ ‘रिसेप्टर्स’ यानी संदेशवाहक होते हैं, जो बाहर से मिलने वाले संकेतों को कोशिका के भीतर पहुँचाते हैं। इन्ही संकेतों के आधार पर कोशिकाएं तय करती हैं कि उन्हें कब बढ़ना है, कब विभाजित होना है और कब खुद को जीवित रखना है। कैंसर जैसी स्थिति तब पैदा होती है जब ये संकेत देने वाले तंत्र खराब हो जाते हैं और कोशिकाएं बिना किसी नियंत्रण के बढ़ने लगती हैं। डॉ. राहुल दास और उनकी टीम ने इसी जटिल प्रक्रिया के एक अत्यंत सूक्ष्म हिस्से को डिकोड किया है, जिससे यह स्पष्ट हुआ है कि एक ‘शांत’ दिखने वाला एंजाइम कैसे कैंसर को रोकने या बढ़ाने में भूमिका निभा सकता है।
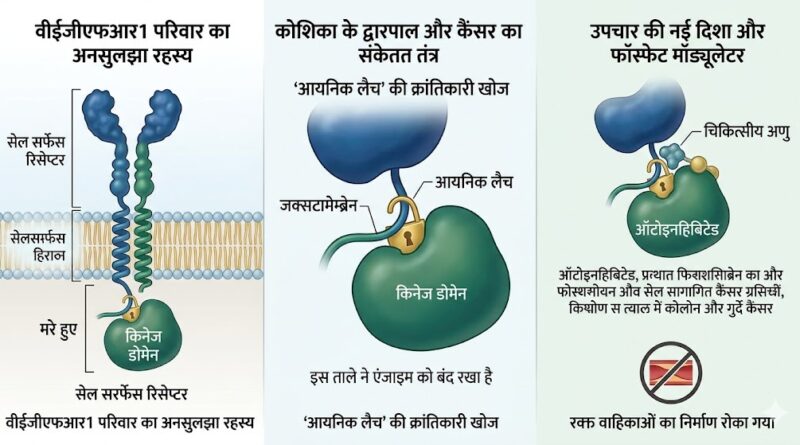
कोशिका के द्वारपाल और कैंसर का संकेत तंत्र
कैंसर की उत्पत्ति और विकास में रिसेप्टर टायरोसिन किनेसेस (RTKs) की भूमिका सबसे महत्वपूर्ण मानी जाती है। ये कोशिका की सतह पर मौजूद ऐसे द्वारपालों की तरह होते हैं जो वृद्धि कारकों (Growth Factors) यानी ‘लिगैंड’ से जुड़ते ही सक्रिय हो जाते हैं। जब ये सक्रिय होते हैं, तो कोशिका के भीतर रासायनिक प्रतिक्रियाओं की एक पूरी श्रृंखला शुरू हो जाती है, जिसे सिग्नलिंग कॉम्प्लेक्स कहा जाता है। यह प्रक्रिया सामान्य परिस्थितियों में घाव भरने, नई रक्त वाहिकाओं के निर्माण और भ्रूण के विकास के लिए आवश्यक है। लेकिन जब ये रिसेप्टर्स बिना किसी बाहरी संकेत के अपने आप सक्रिय होने लगते हैं, तो यह शरीर के लिए विनाशकारी हो जाता है। यही वह स्थिति है जो मधुमेह, स्व-प्रतिरक्षित विकारों और विशेष रूप से कैंसर का कारण बनती है। शोधकर्ताओं के सामने सबसे बड़ा सवाल यह था कि शरीर इन एंजाइमों को ‘ऑफ’ की स्थिति में कैसे रखता है और कैंसर के दौरान यह ‘ऑफ’ बटन काम करना क्यों बंद कर देता है।
वीईजीएफआर परिवार का अनसुलझा रहस्य
वीईजीएफआर (VEGFR) परिवार के सदस्य नई रक्त वाहिकाओं के निर्माण यानी ‘एंजियोजेनेसिस’ की प्रक्रिया को नियंत्रित करते हैं। ट्यूमर को बढ़ने के लिए पोषण और ऑक्सीजन की जरूरत होती है, जिसे वह नई रक्त वाहिकाएं बनाकर प्राप्त करता है। इस परिवार में दो प्रमुख सदस्य हैं: वीईजीएफआर1 और वीईजीएफआर2। अब तक वैज्ञानिक इस बात से हैरान थे कि ये दोनों सगे भाई जैसे होने के बावजूद बिल्कुल अलग व्यवहार करते हैं। वीईजीएफआर2 बहुत ही चंचल है और बिना किसी बाहरी उकसावे के भी खुद-ब-खुद सक्रिय हो जाता है, जिससे कैंसर को बढ़ावा मिलता है। इसके विपरीत, वीईजीएफआर1 एक ‘मरे हुए’ या ‘सुप्त’ एंजाइम की तरह व्यवहार करता है। यह अपने लिगैंड के साथ दस गुना अधिक मजबूती से जुड़ता है, फिर भी यह उतनी जल्दी सक्रिय नहीं होता। आईआईएसईआर कोलकाता के शोधकर्ताओं ने इसी विरोधाभास की गहराई से जांच की और पाया कि वीईजीएफआर1 असल में मृत नहीं है, बल्कि उसने खुद को एक विशेष ‘आणविक ताले’ में बंद कर रखा है।
‘आयनिक लैच‘ की क्रांतिकारी खोज
डॉ. राहुल दास और उनकी टीम ने जिस सबसे महत्वपूर्ण तंत्र की खोज की है, उसे ‘आयनिक लैच’ (Ionic Latch) कहा जाता है। यह एक तरह की विद्युतीय कुंडी है जो केवल वीईजीएफआर1 में पाई जाती है। यह कुंडी एंजाइम के किनेज डोमेन को एक खास स्थिति में जकड़ कर रखती है, जिसे वैज्ञानिक भाषा में ‘ऑटोइनहिबिटेड’ अवस्था कहते हैं। सरल शब्दों में, यह एक सुरक्षा तंत्र है जो एंजाइम को तब तक ‘स्लीप मोड’ में रखता है जब तक कि उसकी वास्तव में आवश्यकता न हो। शोध में पाया गया कि जब यह एंजाइम सक्रिय होता है, तो यह कैंसर से संबंधित दर्द और स्तन कैंसर में ट्यूमर कोशिकाओं के अस्तित्व को बचाने में मदद करता है। कोलन कैंसर के मामलों में, यही एंजाइम कैंसर कोशिकाओं को शरीर के एक हिस्से से दूसरे हिस्से में स्थानांतरित करने यानी ‘मेटास्टेसिस’ के लिए जिम्मेदार होता है। इस ‘आयनिक लैच’ की खोज ने वैज्ञानिकों को वह सटीक स्थान दिखा दिया है जहाँ दवाएं हमला कर सकती हैं।
उपचार की नई दिशा और फॉस्फेट मॉड्यूलेटर
इस शोध का एक अन्य क्रांतिकारी पहलू ‘सेलुलर टायरोसिन फॉस्फेट’ की भूमिका को समझना है। शोधकर्ताओं ने यह प्रस्ताव दिया है कि कोशिका के भीतर मौजूद कुछ विशेष रसायन इस एंजाइम की गतिविधि को नियंत्रित करने में महत्वपूर्ण भूमिका निभाते हैं। आईआईएसईआर कोलकाता की विश्लेषणात्मक जीव विज्ञान सुविधा में अत्याधुनिक उपकरणों की मदद से किए गए प्रयोगों ने यह साबित किया है कि फॉस्फेट मॉड्यूलेटर का उपयोग करके कैंसर के दौरान बनने वाली अवांछित रक्त वाहिकाओं को रोका जा सकता है। यह खोज इसलिए भी महत्वपूर्ण है क्योंकि वर्तमान में उपलब्ध कैंसर की अधिकांश दवाएं सक्रिय एंजाइमों को मारने की कोशिश करती हैं, जिसके अक्सर गंभीर दुष्प्रभाव होते हैं। लेकिन यदि हम वीईजीएफआर1 को उसकी प्राकृतिक ‘शांत’ या ‘ऑटोइनहिबिटेड’ अवस्था में ही स्थिर कर दें, तो कैंसर को बढ़ने से बहुत ही सौम्य तरीके से रोका जा सकता है।
भविष्य की राह और चिकित्सा में बदलाव
अंततः, ‘नेचर कम्युनिकेशंस’ में प्रकाशित यह शोध भविष्य की कैंसर थेरेपी के लिए एक नया ब्लूप्रिंट प्रदान करता है। अब वैज्ञानिक ऐसे छोटे अणुओं (Small Molecules) के निर्माण पर ध्यान केंद्रित कर सकते हैं जो विशेष रूप से वीईजीएफआर1 की उस ‘आयनिक लैच’ वाली स्थिति को मजबूत करें। इससे न केवल कोलन और गुर्दे के कैंसर के इलाज में सुधार होगा, बल्कि यह अन्य प्रकार के कैंसरों के लिए भी उपचार का मार्ग प्रशस्त करेगा जहाँ एंजियोजेनेसिस एक प्रमुख कारक है। यह खोज यह भी स्पष्ट करती है कि प्रकृति ने हमारे शरीर में कैंसर जैसी बीमारियों से लड़ने के लिए पहले से ही कितने जटिल रक्षा तंत्र बनाए हैं। बस जरूरत थी तो उन तंत्रों के काम करने के तरीके को समझने की, जो अब भारतीय वैज्ञानिकों की इस उपलब्धि से संभव हो पाया है। यह शोध न केवल शैक्षणिक दृष्टि से महत्वपूर्ण है, बल्कि यह नैदानिक चिकित्सा (Clinical Medicine) में एक नए युग की शुरुआत कर सकता है जहाँ उपचार अधिक सटीक, प्रभावी और लक्षित होगा। इससे रोगियों के जीवन की गुणवत्ता में सुधार होने की प्रबल संभावना है।
==================================================================
लेख का लिंक: https://doi.org/10.1038/s41467-024-45499-2